创新医疗器械特别审批申请审查结果公示(2018年第13号)
依据国家药品监督管理局《创新医疗器械特别审批程序(试行)》(食药监械管〔2014〕13号)要求,创新医疗器械审查办公室组织有关专家对创新医疗器械特别审批申请进行了审查,拟同意以下申请项目进入特别审批程序,现予以公示。
1.产品名称:高危型人乳头瘤病毒(HPV)E6/E7mRNA检测试剂盒(支链DNA信号扩增法)
申 请 人:郑州科蒂亚生物技术有限公司
2.产品名称:球形聚焦超声组织消融系统
申 请 人:重庆海扶医疗科技股份有限公司
3.产品名称:经导管主动脉瓣膜及可回收输送系统
申 请 人:上海微创心通医疗科技有限公司
4.产品名称:微卫星不稳定性(MSI)检测试剂盒(荧光PCR-毛细管电泳法)
申 请 人:上海普洛麦格生物产品有限公司
公示时间:2018年11月21日至2018年12月5日
公示期内,任何单位和个人有异议的,可以书面、电话、邮件等方式向我中心综合业务处反映。
联系人:李文霞
电话:010-86452913
电子邮箱:gcdivision@cmde.org.cn
地址:北京市气象路50号院1号楼202室
国家食品药品监督管理总局
医疗器械技术审评中心
2018年11月21日
医疗器械优先审批申请审核结果公示(2018年第8号)
依据国家药品监督管理局《医疗器械优先审批程序》(总局公告2016年168号),我中心对申请优先审批的医疗器械注册申请进行了审核。下述项目符合优先审批情形,拟定予以优先审批,现予以公示。
|
序号 |
受理号 |
产品名称 |
申请人 |
同意理由 |
|
1 |
JSZ1800102 |
抗PD-L1 (SP142)兔单克隆抗体试剂(免疫组织化学法) |
Roche Diagnostics GmbH |
诊断或者治疗恶性肿瘤,且具有明显临床优势;临床急需,且在我国尚无同品种产品获准注册的医疗器械。 |
|
2 |
JQZ1800416 |
镍钛合金紫杉醇洗脱血管支架 |
Boston Scientific Corporation |
临床急需,且在我国尚无同品种产品获准注册的医疗器械。 |
公示时间:2018年11月21日至2018年11月28日
公示期内,任何单位和个人有异议的,可以填写医疗器械优先审批项目异议表,书面提交至我中心综合业务处。
联系人:李文霞
电话:010-86452913
电子邮箱:gcdivision@cmde.org.cn
地址:北京市气象路50号院1号楼202室
国家食品药品监督管理总局
医疗器械技术审评中心
2018年11月21日
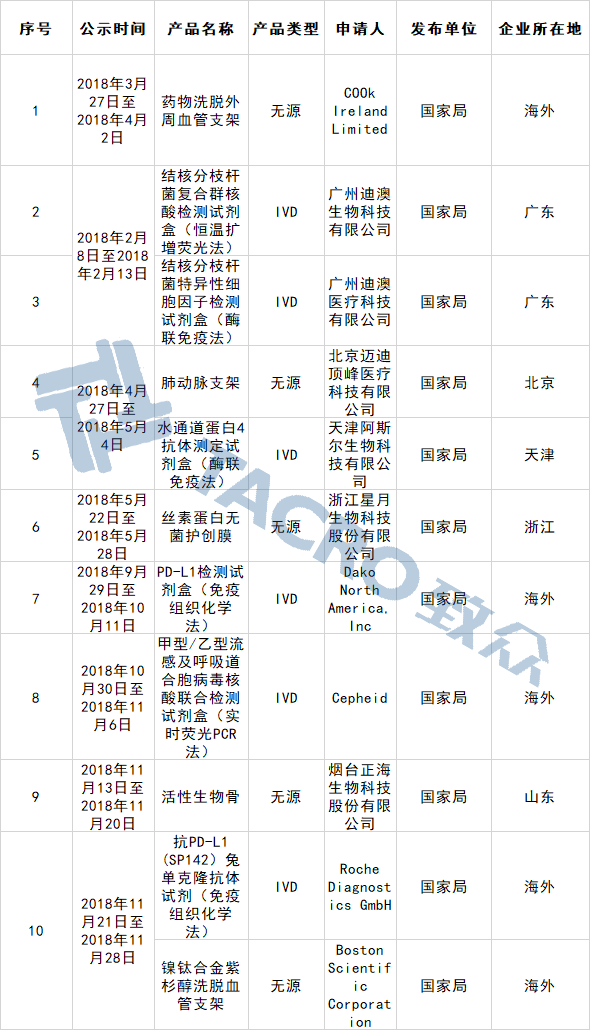
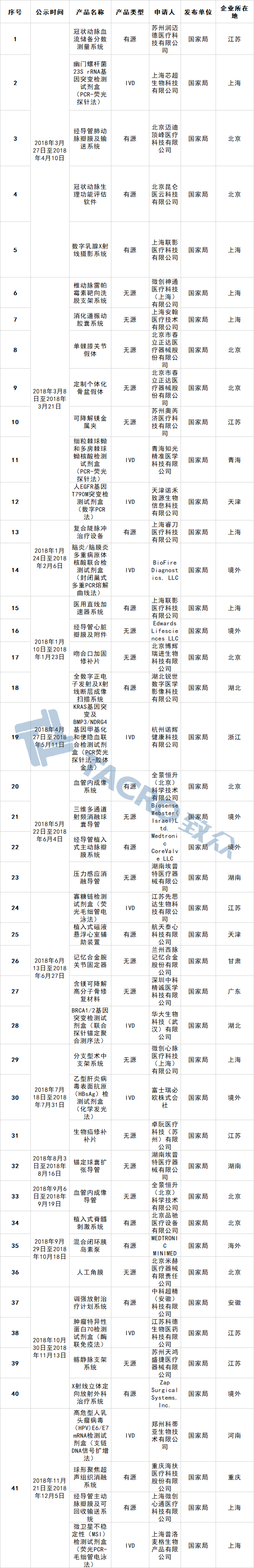
以下是致众整理的2018年创新与优先审批汇总:
创新:
优先: