关于发布2018年第二批医疗器械临床试验监督抽查项目的通告(2018年第119号)
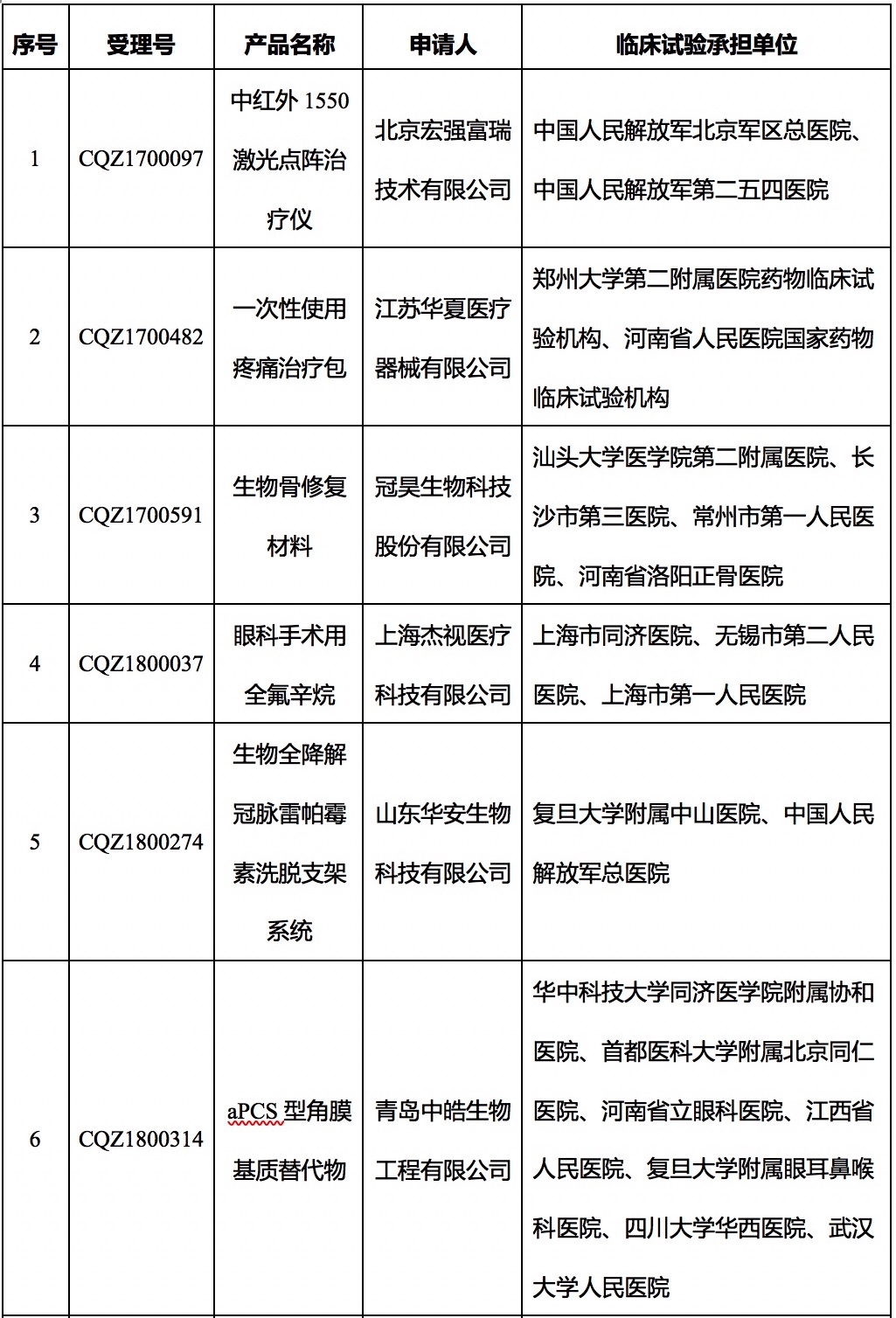
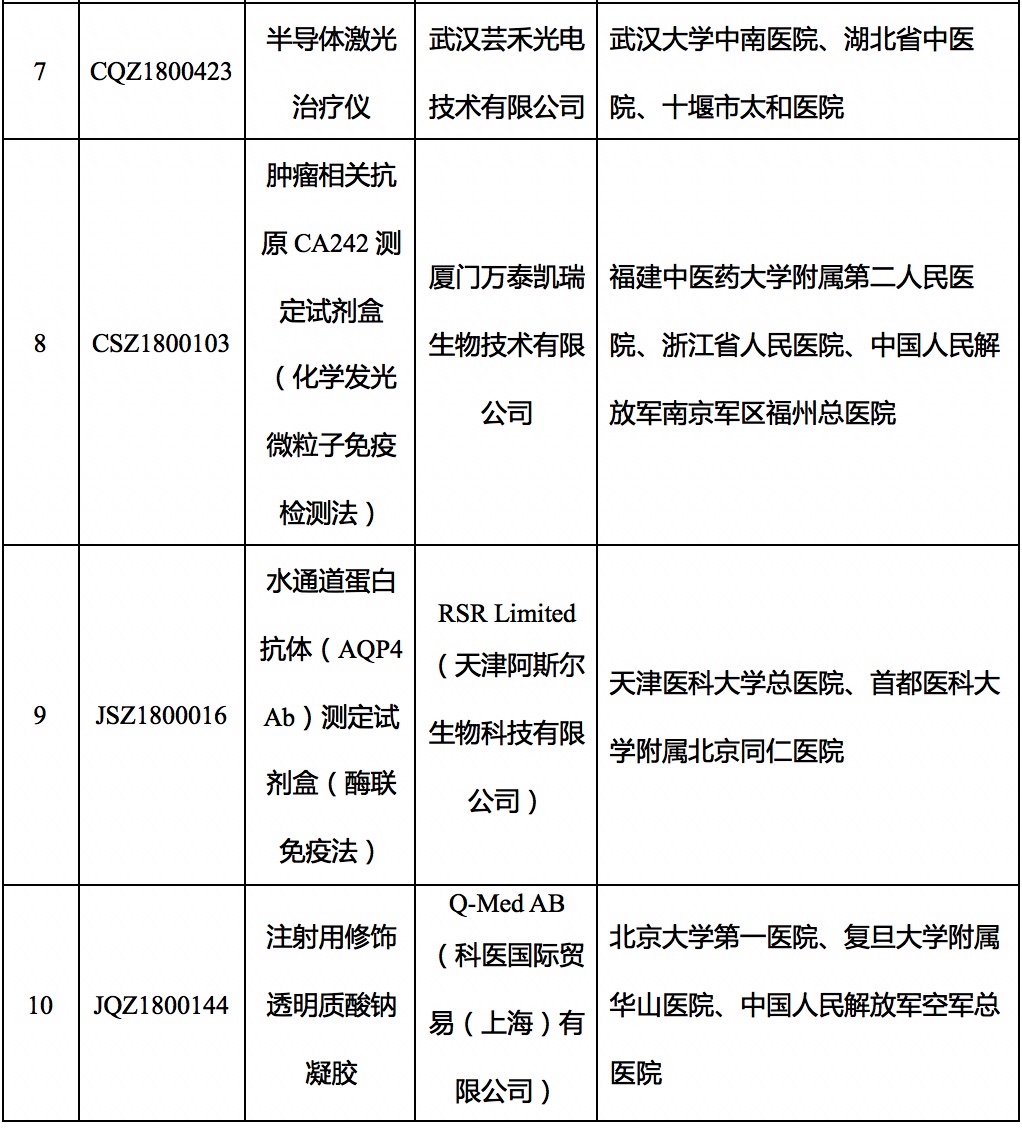
为贯彻实施中共中央办公厅、国务院办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号),加强医疗器械临床试验监督管理,根据2018年重点工作安排,国家药品监督管理局抽取中红外1550激光点阵治疗仪(受理号:CQZ1700097)等10个注册申请项目,将对其临床试验数据的真实性、合规性组织开展现场监督检查。注册申请项目受理号、产品名称、申请人及临床试验承担单位见附件。具体检查时间安排和抽查的临床试验机构由国家食品药品监督管理总局食品药品审核查验中心另行通知。
自本通告发布后,不再受理注册申请人对上述项目的自行撤回申请。
特此通告。
附件:2018年第二批医疗器械临床试验监督抽查项目
国家药监局
2018年11月23日
附件
2018年第二批医疗器械临床试验
监督抽查项目